Problema n° 4 de gases ideales - TP02
Enunciado del ejercicio n° 4
Un tubo cilíndrico de 1,5 m de largo se sumerge verticalmente en mercurio hasta que el extremo cerrado queda a 25 cm de la superficie libre del mercurio. Determinar la longitud que ocupará, dentro del tubo, el aire, si la presión exterior es de 75 cm de Hg (δ = 13,56 g/cm³).
Desarrollo
Datos:
l = 1,5 m
Δl = 25 cm = 0,25 m
p = 75 cm Hg
| p = | 101.325 Pa·75 cm Hg |
| 76 cm Hg |
p = 99.991,7763 Pa
δ = 13,56 g/cm³
| δ = 13,56 g/cm³· | 1 kg | · | 1.000.000 cm³ |
| 1.000 g | 1 m³ |
δ = 13.560 kg/m³
Fórmulas:
| p1·V1 | = | p2·V2 |
| T1 | T2 |
Esquema:
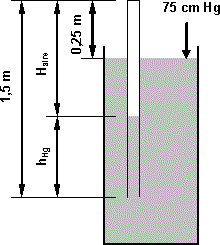
Esquema del barómetro
Solución
Aplicamos la ecuación general de los gases ideales. Para el caso:
p1·V1 = p2·V2
Pero el volumen es:
p1·π·r²·h1 = p2·π·r²·h2
Como la sección es uniforme:
p1·h1 = p2·h2
| h2 = | p1·h1 | (1) |
| p2 |
Siendo:
h1: 1,50 m
h2: la altura buscada.
p1: es la presión inicial, la atmosférica.
p2: es la presión final, presión que el aire ejerce sobre el mercurio.
Según el esquema y el enunciado la presión en la boca del tubo es:
p = p0 + δ·g·h
Donde:
p0: es la presión atmosférica (p1).
h: es la altura del mercurio (1,25 m).
Siendo g = 9,80665 m/s²
p = 99.991,7763 Pa + (13.560 kg/m³)·(9,80665 m/s²)·1,25 m
p = 266.214,494 Pa
Esta presión se encuentra equilibrada con la interna del tubo, que esta ejercida por el aire. Aplicando la ecuación (1):
| h2 = | p1·h1 |
| p2 |
| h2 = | 99.991,7763 Pa·1,50 m |
| 266.214,494 Pa |
Resultado, la longitud que ocupará el aire es:
h2 = 0,5634 m
Autor: Ricardo Santiago Netto. Argentina
Ejemplo, cómo calcular la presión de un gas con el cambio de volumen