Principios de la electrólisis
Es la parte de la química que trata de la relación entre las corrientes eléctricas y las reacciones químicas, y de la conversión de la energía química en eléctrica y viceversa. En un sentido más amplio, la electroquímica es el estudio de las reacciones químicas que producen efectos eléctricos y de los fenómenos químicos causados por la acción de las corrientes o voltajes.
Conductores de Corriente Eléctrica
Cualquier material que ofrezca poca resistencia al flujo de electricidad se denomina conductor eléctrico, como las disoluciones de la mayoría de los ácidos inorgánicos, bases y sales son buenos conductoras de la electricidad y todo material que impida el paso de la corriente eléctrica es denominado mal conductor o aislador eléctrico, como las disoluciones de azúcar, alcohol, glicerina y muchas otras sustancias orgánicas. La diferencia entre un conductor y un aislante, es de grado más que de tipo, ya que todas las sustancias conducen electricidad en mayor o en menor medida. Un buen conductor de electricidad, como la plata o el cobre, puede tener una conductividad mil millones de veces superior a la de un buen aislante, como el vidrio o la mica. En los conductores sólidos la corriente eléctrica es transportada por el movimiento de los electrones; y en disoluciones y gases, lo hace por los iones.
Los conductores se clasifican en:
a. Conductores de 1° clase: son aquellos que dejan fluir la electricidad sin sufrir alteración, como los metales.
b. Conductores de 2° clase o electrólitos: son aquellos que se ionizan y entonces conducen la corriente eléctrica, como las soluciones acuosas de ácidos, bases y sales, así también las sales fundidas.
Los electrólitos a su vez se clasifican en:
1) Los electrólitos que proporcionan disoluciones altamente conductoras se llaman electrólitos fuertes (como el ácido nítrico o el cloruro de sodio).
2) Débiles: Los que producen disoluciones de baja conductividad reciben el nombre de electrólitos débiles como el cloruro mercurioso (HgCl2) o el ácido etanoico (CH3—COOH).
Conductores
| Conductores de | 1° clase | |
| 2° clase o electrólitos | Fuertes Débiles | |
| Malos conductores o aislantes | ||
Electrólitos
Los ácidos, sales las bases y las sales sólidas son malos conductores de la electricidad, pero cuando cualquiera de estas sustancias se disuelve en agua, la solución resultante es conductora.
Cuando una de estas sustancias se disuelve en agua (o se funde) se disocian en partículas con carga eléctrica (positiva o negativa) llamadas iones y a la disociación en iones se la denomina ionización. Así un ion se define como átomo o grupo de átomos con carga eléctrica. Un átomo que pierde un electrón forma un ion de carga positiva, llamado catión; un átomo que gana un electrón forma un ion de carga negativa, llamado anión.
Cualquier sustancia que produce iones en solución es un electrólito. Las sales son iónicas aún en estado sólido, pero cuando se disuelven o se funden, los iones se separan y adquieren libertad de movimiento. La conducción electrolítica se debe a la movilidad iónica en estado líquido.
Ionización
Al combinarse sodio con cloro, para formar cloruro de sodio, cada átomo de sodio cede un electrón a un átomo de cloro, dando como resultado un ion sodio con carga positiva y un ion cloro con carga negativa.
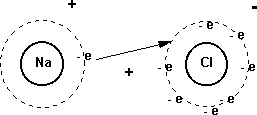
Formación del enlace iónico entre el sodio y el cloro
Cl2° + 2·Na° ⟶ 2·NaCl
En un cristal de cloruro de sodio la fuerte atracción electrostática entre iones de cargas opuestas mantiene firmemente los iones en su sitio, estableciéndose un enlace iónico. Cuando el cloruro de sodio se disuelve en agua, los iones se disocian y pueden moverse libremente.
NaCl ⟶ Na+ + Cl¯
Cuando se disuelve cloruro de sodio en agua, los iones se disocian (por la atracción entre los iones y el disolvente), y esta disolución es un excelente conductor de la electricidad.
El químico sueco Svante August Arrhenius fue el primero en descubrir que algunas sustancias en disolución se encuentran en forma de iones y no de moléculas, incluso en ausencia de una diferencia de potencial eléctrico. Cuando un electrólito se introduce en una disolución, se disocia parcialmente en iones separados, y que el grado de disociación depende de la naturaleza del electrólito y de la concentración de la disolución. Según la teoría de Arrhenius, al disolver una determinada cantidad de cloruro de sodio en un gran volumen de agua, los iones se disocian en mayor grado que si esa misma cantidad se disuelve en un volumen menor de agua.
La teoría de Debye-Hückel afirma que los electrólitos están totalmente disociados en una disolución. La tendencia de los iones a emigrar y conducir la electricidad queda retardada por las atracciones electrostáticas entre los iones de cargas opuestas y entre los iones y el disolvente. A medida que aumenta la concentración de la disolución, se incrementa el efecto retardante. Así, una cantidad fija de cloruro de sodio resulta mejor conductor si se disuelve en un gran volumen de agua, al encontrarse los iones más apartados entre sí, ejerciendo una atracción menor respecto a los demás y respecto a las moléculas del disolvente. Sin embargo, los iones no tienen libertad total para emigrar.
La constante dieléctrica del disolvente es otro factor importante en las propiedades de la disolución. La ionización es mayor en un disolvente como el agua, que tiene una constante dieléctrica elevada.
Autor: Ricardo Santiago Netto. Argentina
¿Qué es un electrolito? ¿Cómo se define a un catión y un anión?