Ejemplo n° 1 de fuentes de energía
Ejemplo nº 1
Calentar 1 kg de agua de 10 °C a 100 °C. ¿Qué cantidad de calor sensible se le ha agregado?
Solución
Si:
Q = m·cₑ·(t°f - t°ᵢ) ⇒ Q = 1 kg·1 kcal/kg·°C·(100 °C - 10 °C) ⇒ Q = 90 kcal
Sin embargo, sucede que cuando se esta materializando un cambio de estado físico, se verifica que el agregado o sustracción de calor no origina variación de temperatura. En efecto, por ejemplo, si se tiene agua en ebullición, durante todo el proceso que esta dura, la temperatura se mantiene constante en los 100 °C, aunque se le agregue calor continuamente.
A ese calor que agregado a una sustancia no origina cambio de nivel térmico o temperatura, se lo denomina calor latente, o sea, como su nombre lo indica, ese calor se encuentra latente, y se consume en la acción de transformación física.
Q = m·cᵥₗ
Donde:
Cᵥₗ es el calor latente de vaporización (kcal/kg)
El calor latente de vaporización del agua (100 °C) es 539 kcal/kg
El calor latente de fusión del agua (0 °C) es 80 kcal/kg
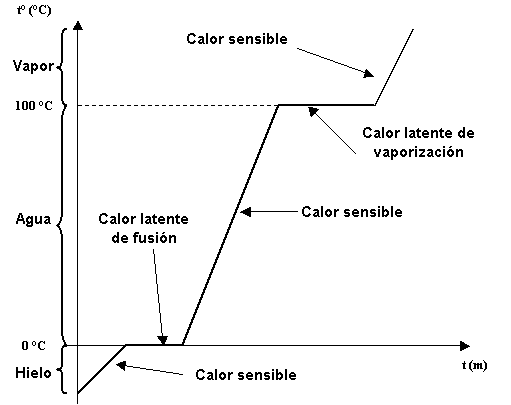
Gráficos del calor sensible y el calor latente
Resolvió: Ricardo Santiago Netto. Argentina
Ejemplo, cómo calcular el calor sensible