Problema nº 1 de composición atómica, relación entre el volumen del átomo y el del núcleo - TP02
Enunciado del ejercicio nº 1
El radio aproximado del átomo de hidrógeno es de 0,0529 nm y el del protón es de 1,50·10⁻⁶ nm. Calcular la relación entre el volumen del átomo y el del núcleo, suponiendo a ambos esféricos.
Dato: volumen de la esfera = 4/3·π·r³
Desarrollo
Datos:
rₐ = 0,0529 nm
rₚ = 1,50·10⁻⁶ nm
Fórmulas:
![]()
Solución
Nos pide la siguiente relación:
![]()
Reemplazamos por la fórmula de volumen:
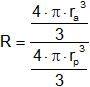
Simplificamos:
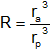
Reemplazamos por los datos y calculamos:
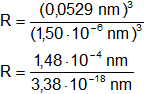
Respuesta, la relación entre el volumen del átomo y el del núcleo es:
R = 4,39·10¹³
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP02
- | Siguiente ›
Ejemplo, cómo determinar la relación entre el volumen del átomo y el del núcleo