Las fórmulas de las sustancias
Fórmula mínima de las sustancias
La fórmula mínima de una sustancia representa la composición de esta con el menor número posible de átomos de los elementos que forman su molécula.
El número de átomos de cada elemento se indica con un subíndice escrito en la parte inferior derecha del elemento.
Cálculo de la fórmula mínima
Para ello partiremos de la composición centesimal, que dice: la composición centesimal de una sustancia indica la masa de cada uno de los elementos que hay en 100 g de esa sustancia.
Por ejemplo, se tiene la siguiente composición centesimal:
| Elemento | Porcentaje (%) | Átomo gramo (g) |
|---|---|---|
| C | 37,5 | 12,0 |
| H | 5,2 | 1,0 |
| O | 33,4 | 16,0 |
| Na | 23,9 | 23,0 |
| 100 | - |
El 100 % de la composición se corresponden con 100 g por ser el total.
Primero calculamos el número de átomos gramo que hay en 100 g de sustancia:
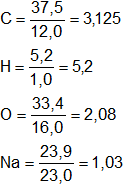
El número de átomos gramo de cada elemento debe ser entero, podemos despreciar los decimales o dividir a todos por el menor átomo gramo de los obtenidos.
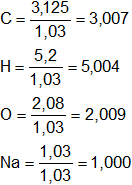
Ahora sí despreciamos los decimales.
| Elemento | Porcentaje (%) | Átomo gramo (g) |
|---|---|---|
| C | 37,5 | 3 |
| H | 5,2 | 5 |
| O | 33,4 | 2 |
| Na | 23,9 | 1 |
| 100 | - |
Presentamos la fórmula mínima:
C₃H₅O₂Na₁
Los subíndices son siempre números enteros dado que los átomos no son divisibles.
Fórmula molecular de las sustancias
La fórmula molecular de una sustancia expresa el número de átomos gramo de cada elemento que hay en el mol de esta sustancia.
Cálculo de la fórmula molecular
Continuando con la fórmula mínima hallada:
C₃H₅O₂Na
Podemos presentar las siguientes fórmulas donde los elementos guardan la misma relación:
C₆H₁₀O₄Na₂
C₉H₁₅O₆Na₃
Para generalizar:
(C₃H₅O₂Na)ₙ
Debemos definir cuál es la fórmula molecular de la sustancia. Para ello debemos conocer el peso molecular de dicha sustancia para determinar el valor de n.
Procedemos:
a) Se calcula el peso molecular gramo:
| Elemento | Subíndice | Átomo gramo (g) | Total (g) |
|---|---|---|---|
| C | 3 | 12 | 36 |
| H | 5 | 1 | 5 |
| O | 2 | 16 | 32 |
| Na | 1 | 23 | 23 |
| 96 | |||
b) Se halla el peso molecular de la sustancia, supongamos que es igual 192 g.
c) Hallamos el valor de n:
![]()
d) La fórmula molecular de la sustancia dada es:
(C₃H₅O₂Na)₂
C₆H₁₀O₄Na₂
Bibliografía:
Héctor Fernández Serventi. "Química general e inorgánica". Losada S. A., Buenos Aires.
Robert C. Smoot y Jack Price. "Química, Un curso moderno". Compañía Editorial Continental S. A., México.
Autor: Ricardo Santiago Netto. Argentina
Fórmula mínima y molecular