Proteínas: La célula
La célula
Unidad estructural y funcional de los seres vivos más pequeña. Hay organismos unicelulares y esta célula debe hacer todas las funciones que caracterizan al organismo. Hay organismos pluricelulares con millones de células especializadas que en origen son iguales y luego se especializan aunque tengan el mismo DNA. La característica básica de la célula es la membrana que le da individualidad respecto del medio. A ambos lados de la membrana la composición es distinta y mantener ese estado cuesta energía. Las células pueden tener gran diversidad de tamaños, desde 0,5 µm hasta centímetros. Las células se clasifican en:
Procariotas:
Bacterias, carecen de compartimentos interiores, ni siquiera para el DNA.
Eucariotas:
Más complicadas y grandes, tienen muchos orgánulos y compartimentos de membrana definida. La composición de cada compartimento es definida.
Morfología de las procariotas:
- Membrana plasmática: rodea a la célula manteniendo la individualidad. Hay muchos transportadores para meter o sacar moléculas. Además tiene la función de producir energía creando un gradiente de concentración para que cuando se deshaga usar esa energía. Para crear este gradiente se usa energía procedente de nutrientes o del sol.
- Pared celular: típica de procariotas, da rigidez, protege frente a daños e hinchamiento osmótico. Está constituida por polisacáridos.
- Citoplasma: parte interior de la membrana, donde están el resto de componentes celulares: proteínas, casi todos los enzimas, ribosomas … El DNA en procariotas tiene una estructura fibrosa irregular y es de forma circular.
- Ribosomas: partículas formadas por proteínas y ácidos nucleicos que sintetizan proteínas.
- Pili: filamentos cortos empleados en la adhesión.
- Filamentos: movimiento celular y citoesqueleto.
Morfología de las eucariotas:
- Membrana plasmática: permite entrada o salida de componentes mediante multitud de transportadores específicos. Así mismo tiene muchos receptores de señales. No está relacionada con la producción de energía.
- Núcleo: contiene el DNA. Tiene una membrana con muchos poros para dejar entrar o salir cosas.
- Nucleolo: más denso, síntesis de subunidades de ribosomas.
Formaciones membranosas.
- Retículo endoplásmico: serie de sacos membranosos.
- Aparato de Golgi
Ambos son importantes para la síntesis, clasificación y secreción de muchas proteínas.
- Mitocondrias: es donde se fabrica mayor cantidad de energía (ATP) en la célula. La membrana interna de las mitocondrias es igual a la membrana plasmática de los procariotas. Membrana interior presenta múltiples pliegues y se supone que parasitaban células hasta que se integraron, pues poseen su propio DNA para sintetizar sus proteínas.
- Lisosomas: bolsas de pH muy ácido donde se hidrolizan los compuestos.
Vegetales:
La fotosíntesis se localiza en la membrana en el caso de procariotas y en los cloroplastos en las eucariotas.
Diferencias con células animales:
- Son fotosintéticas
- Poseen vacuolas que son grandes sacos membranosos que sirven para almacenar pigmentos, proteínas
- Normalmente poseen pared celular
Ancestro común:
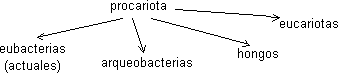
Se supone que había un procariota a partir del cual se originaron todos los demás.
El agua
La vida transcurre en un entorno acuoso, la célula puede tener hasta un 70-90 % de agua. El agua rellena todos los huecos. Un eritrocito estaría formado por:
- 80 moléculas de hemoglobina
- 1.000 moléculas orgánicas más pequeñas
- 3.000 iones
- 500.000 moléculas de agua
El agua determina la estructura tridimensional de las moléculas funcionales como proteínas y ácidos nucleicos, que son polímeros formados por monómeros unidos por enlaces covalentes. Los enlaces no covalentes son muy importantes por:
- Dan la estructura tridimensional a las moléculas funcionales, de la cual depende su función
- Contacto temporal entre moléculas para interaccionar. Como es débil se forman y se rompen continuamente
Interacciones débiles:
1) Iónicas:
Atracción o repulsión entre moléculas de cargas iguales. La fuerza viene dada por:
F = q₁·q₂/r²·ε
donde ε es la constante dieléctrica del medio.
La ε del agua es muy alta por lo que F no es muy grande a pesar de que dentro de las débiles son fuertes. Este tipo de interacción es importante pues cuando las cargas están muy cerca. Se dan entre moléculas cargadas, entre dipolos y moléculas o entre dos dipolos. (inducidos o no). No son direccionales
2) Fuerzas de Van der Waals:
Son más débiles que las anteriores y sólo se dan entre moléculas muy próximas o apiladas. Se inducen dipolos por proximidad. A pesar de ser débiles son capaces de mantener dos cadenas juntas por que hay muchas interacciones, como ocurre con las colas hidrocarbonadas en las membranas
3) Puentes de hidrógeno:
Es la más fuerte de todas las interacciones. Se establece entre un hidrógeno unido covalente-mente a un átomo electronegativo (como O o N) de manera que el enlace está polarizado y el hidrógeno tiene densidad de carga positiva. A este grupo se le denomina dador de puente de hidrógeno. Este enlace se establece con elementos que tienen pares de electrones por compartir como O y N. Se pueden formar entre grupos de la misma molécula o entre moléculas distintas. Las bases nitrogenadas tienen grupos aceptores y dadores en la misma molécula y en moléculas distintas. Como hay muchos puentes las moléculas son muy estables. La estructura helicoidal de las proteínas está sustentada por puentes de hidrógeno
4) Hidrofóbicas:
aquellas partes de la molécula que no son solubles en agua se esconden del entorno acuoso e interactúan entre ellas con fuerzas de tipo Van der Waals
Molécula del agua
Puede tener dos tipos de interacciones débiles:
- Los hidrógenos están polarizados y puede ser dador y el oxígeno tiene dos pares de electrones desapareados por lo que puede ser aceptor
- Como es un dipolo puede tener interacciones iónicas
Puede establecer puentes de hidrógeno entre ella misma o con otras moléculas. Una misma molécula de agua puede ser dadora de 2 puentes y aceptora de 2 más, cuatro en total. Por ello cuesta mucho cambiar su estado. En estado sólido cada molécula forma 4 puentes de hidrógeno dada la disposición tridimensional tetraédrica, muy rígida. En este estado quedan huecos en la red tridimensional. Para cambiar su estado se ha de aportar más calor del normal porque hay que romper los puentes. En estado líquido también forma puentes, pero menos, por lo que el calor de vaporización es también alto. Los huecos quedan rellenados.
Importancia para la vida:
Los huecos en el líquido están ocupados por agua, pero en el hielo no, por lo que es menos denso y flota. Gracias a esto en zonas muy frías se forma una capa de hielo en la superficie y bajo hay agua líquida y puede haber vida. Además el hielo aísla.
Que el calor de vaporización sea muy alto tiene dos ventajas:
1) A temperatura normal el agua es líquida lo que da a las moléculas un entorno fluido para que se muevan
2) Como al evaporarse absorbe calor en la sudoración se consigue rebajar la temperatura corporal
Cuesta cambiar la temperatura del agua porque cuesta agitar las moléculas. Esto es importante porque los seres vivos son muy dependientes de la temperatura y así se mitigan las variaciones.
Para que puedan moverse en un entorno acuoso las moléculas deberán ser solubles, sino precipitan y se tapan unas a otras disminuyendo la variación. Las que forman puentes de hidrógeno o interacciones iónicas son solubles en agua (hidrofílicas) y esto es importante porque la célula está llena de agua. Ser hidrófobo en medio acuoso es desfavorable y tienden a aislarse del agua aumentando la entropía. Si una molécula tiene una parte hidrofílica y otra hidrofóbica se plegará sobre sí misma. Las hidrofóbicas más importantes están en la membrana. Los fosfolípidos que tienen una cabeza polar y una cola apolar se dispone de tres maneras distintas:
- Monocapa: La parte polar se mantendrá cerca del agua y la apolar fuera
- Micelas: al agitarlas se dispongan con las colas hacia dentro y la cabeza fuera
- Bicapa: se disponen de manera que las colas están en contacto y sólo las cabezas tocan el agua, es la misma estructura que una membrana
Editor: Ricardo Santiago Netto (Administrador de Fisicanet).