Proteínas: Funciones
Funciones
En general todas las de la célula:
- Catalizadores: aceleran las reacciones varios órdenes de magnitud
- Estructural: gracias a su estructura fibrosa
- Movimiento de las células: como es el caso de los músculos
- Transmisión del impulso nervioso: el receptor es una proteína
- Transporte: uniéndose a sustancias más pequeñas como la hemoglobina y el oxígeno
- Almacén: en la hemoglobina el O es estable unido al Fe
- Defensa: los anticuerpos son proteínas
- Reguladores: regula expresión del DNA, tiene un papel importante en el crecimiento y diferenciación de las células
Estructura
Son polímeros de aminoácidos unidos por enlaces peptídicos. Algunas tienen entre 50 y 2.500 aminoácidos. Como hay 20 aminoácido hay muchas variaciones: 20ⁿ donde n es el número de monómeros. Desde el punto de vista estructural lo más importante es que tiene estructura tridimensional. De todas las maneras posibles sólo se ordena de la forma que sea más estable termodinámicamente. Para que funcionen tienen que tener estructura tridimensional, estar en conformación nativa. La desnaturalización es la pérdida de estructura tridimensional, la cadena de aminoácidos está igual pero no funciona, está hidrolizada.
Aminoácidos
α-aminoácidos:
Son los monómeros constituyentes. En el carbono α tienen un grupo amino y un grupo carboxilo. El carbono es α porque está al lado del carbono más oxidado. Los otros 2 sustituyentes son un hidrógeno y una cadena lateral R. Como hay 20 R distintos hay 20 aminoácido diferentes. Según R el aminoácido tendrá unas propiedades u otras. A pH celular (7) el grupo carboxilo está disociado (implica carga negativa) y el amino protonado. Aunque R no interaccione con agua los otros grupos sí.
Cadenas laterales:
Apolares: no tienen tendencia a interaccionar con el agua iónicamente o por puentes de hidrógeno.
1) Cadena alifática: alanina, valina, leucina, isoleucina
2) Anillo aromático: fenilalanina, triptófano
3) Azufre en R: metionina
4) Prolina: La cadena lateral se une al grupo amino del aminoácido formando una anillo
Polares: una cadena polar tiene grupos que interaccionan con el agua. A pH fisiológico pueden estar cargados o no.
No cargados:
- Glicina
- Hidroxilo: serina, treonina, tirosina
- Sulfhidrilo: cisteína, es importante porque sufre interacciones que no padece ningún otro, porque se puede establecer un puente bisulfuro entre las cadenas laterales
- Amida: glutamina y asparagina. Son derivados de dos aminoácido ácidos (glutámico y aspártico)
Cargados negativamente:
Tienen una carga negativa en la cadena lateral como tienen un grupo carboxilo son aminoácido ácidos.
Aminoácido ácidos: aspártico (β-carboxilo) y glutámico (γ-carboxilo).
Los amidas son amidas de éstos ácidos.
Cargados positivamente:
- Amino: lisina (ε-amino)
- Imidazol: histidina
- Guanidíneo: arginina (es el más fuerte como base, para disociarlo debe estar a pH 12 por lo que difícilmente pierde la carga positiva)
Estos aminoácido son codificables porque en el DNA existe información distinta para cada uno (están codificados en los codones). Otros aminoácido entran a formar parte de la proteína pero no son codificables y son modificaciones de los 20 aminoácido. Son derivados hidroxilados, en concreto hay 2 importantes: hidroxilisina e hidroxiprolina. Para que una proteína tenga hidroxilaciones el DNA pone el aminoácido y cuando ya forma parte de la cadena una enzima lo modifica (modificación post-traduccional). Además existen aminoácido no proteicos que no forman parte de las proteínas, cumplen funciones antibióticas, pared celular, transmisión del impulso nervioso … A veces ni siquiera son α-aminoácidos. La tiroxina es una hormona que es un derivado de la tirosina.
Propiedades de los aminoácidos
Todos menos la glicina tienen 4 sustituyentes distintos en el carbono α por lo que tienen un centro quiral y pueden existir en formas estereoisómeras (imágenes especulares), tienen actividad óptica y pueden ser levorrotatorios o dextrorrotatorios. Si hay otro carbono quiral habrán más estereoisómeros. Menos treonina e isoleucina los demás tienen sólo un carbono α. Para pasar de un configuración a otra se han de romper enlaces. Para distinguir la configuración alrededor del carbono α se les llama L y D. Colocando el grupo carboxilo en el centro si NH₃ se queda a la derecha es D-aminoácido. Todos los aminoácido de las proteínas son L. Todas las moléculas que tienen formas estereoisómeras en la Naturaleza se presentan sólo en una forma. Si sintetizamos una mezcla de aminoácido habrán L y D al 50 %. Pero como las moléculas han de encajar para reaccionar se ha escogido sólo la forma L. Sí existen D-aminoácido pero no forman parte de las proteínas.
Propiedades ácido base:
A pH fisiológico el grupo carboxilo está disociado y el amino tiene carga positiva. Puede actuar como ácido cediendo el grupo amino un protón y como base aceptándolo el grupo carboxilo. El estado de disociación depende del pH al que se encuentre la disolución y lo fuerte que sea el ácido, habiendo muy fuertes y muy débiles. Independientemente de la cadena lateral tienen 2 grupos disociables, el α-amino y el α-carboxilo. Para tener el aminoácido totalmente protonado el pH debe ser muy ácido. La tendencia a disociarse viene dada por el pK (pK más pequeño, ácido más fuerte). Como el carboxilo tiene pK más bajo que el amino se disocia antes. Al aumentar el pH se disocia primero α-carboxilo y luego el amino.
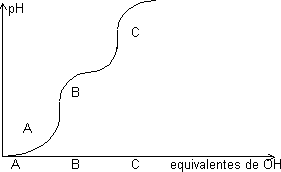
Curva de valoración:
Un aminoácido con dos grupos disociables presenta una curva de valoración con dos saltos. Hay una zona en la que el pH está amortiguado en torno al valor de pK, donde las concentraciones de ambas especies son comparables. Ecuación de Henderson-Hasselback:
![]()
El primer punto de equivalencia es el punto isoeléctrico donde el aminoácido tiene carga eléctrica neutra, A tiene +1 y C -1. Cuando pH < pK predomina la forma no disociada.
Los aminoácido que tienen otro grupo disociable en la cadena lateral son los cargados. El aspártico y el glutámico tienen otro carboxilo:
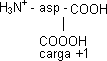 | ⟶ pKACOOH ⟶ | H₃N⁺ | 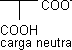 | ⟶ pK RCOOH ⟶ |
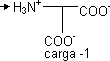 | ⟶ | H₂N | 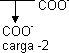 | |
| H₃N⁺ - asp-COOH | pK α COOH | H₃N⁺ | COO⁻ | pK RCOOH |
Cálculo del punto isoeléctrico:
Semisuma de los pK de los equilibrios que tiene a los dos lados la forma isoeléctrica, en este caso:
PI = (pKαCOOH + pKRCOOH)/2
pKs más usuales:
α-COOH: < 3
α-N⁺H₃: 4
Cadena lateral:
ε-N⁺H₃: 10
COOH:4
N⁺H₃: 10
Imidazol: 6
Guanidíneo: 12
Tirosina: 10
Cisteína: 8,5
La histidina es el único aminoácido que es tampón a pH fisiológico porque se disocia.
Estado de disociación de un tripéptido:
Lys-Asp-His
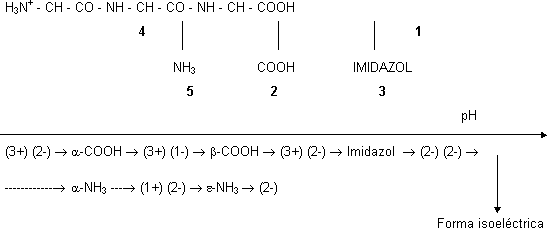
PI = (Imidazol + α-NH₃)/2
La solubilidad de una proteína es mínima en el punto isoeléctrico porque como las moléculas ya no se repelen se asocian formando agregados.
Enlace peptídico
Es de naturaleza covalente, por lo tanto, muy estable. Se forma por condensación entre un α-COOH y el α-N⁺H₃ siguiente:
H₃⁺N—CH—COO⁻ + H₃⁺N—CH—COO⁻ ⟶ —CO—HN - ……
Es un enlace tipo amida en el que se pierde una molécula de agua. Al unir un tercer aminoácido se une igual, por lo que todos los α-COOH y α-NH₃ están implicados en el enlace y dejan de ser operativos todos menos los dos de los extremos. Al α-NH₃ del final de le denomina N-terminal y al α-COOH C-terminal. Los péptidos se ordenan representando primero al aminoácido que tenga el N-terminal libre. Si hay hasta 10 aminoácido se llama oligopéptido. Los polímeros son lineales, como no tienen más grupos para formar enlaces no se ramifican. A cada aminoácido se le llama residuo.
Nomenclatura de péptidos: Todos menos el último acaban en -il y el último permanece igual.
Características del enlace peptídico:
- El esqueleto covalente es siempre el mismo y sólo varían las cadenas laterales. También es importante la secuencia, el orden que llevan
- Es más corto que un enlace sencillo pero más largo que uno doble, carácter parcial de doble enlace. Se suponen dos formas resonantes de enlace simple y doble:
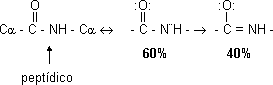
Como es doble no puede girar en torno suyo. Sólo gira el enlace simple del C α, lo que da lugar a isómeros cis - trans de los cuales la forma más estable es la trans. La forma trans tiene un impedimento estérico. En la forma trans los C α están lo más alejados posible. Como el O es más electronegativo que el N el enlace está polarizado. El grupo NH del peptídico no se disocia a ningún pH. 2 grupos pueden formar parte de un puente de hidrógeno, el carbonilo (C=O) sería aceptor y el NH dador. El C del carbonilo tiene 3 sustituyentes dirigidos hacia los vértices de un triángulo en el mismo plano. De este modo, la cadena polipeptídica está formada por una serie de planos que giran alrededor de los C α. Plano rígido:
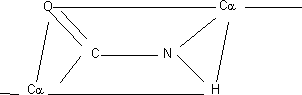
Editor: Ricardo Santiago Netto (Administrador de Fisicanet).