Problema nº 5 de electrólisis. Concentración y ka dada la constante de ionización - TP05
Enunciado del ejercicio nº 5
¿Cuál es la concentración del ion hidronio de una solución de KHSO₄ 0,1 M? Consulte el valor de kₐ en la tabla de constantes de ionización.
Solución
Expresamos la ecuación balanceada de disociación:
KHSO₄ + H₂O ⇌ H₃O⁺ + KSO₄⁻
Planteamos los moles iniciales y en el equilibrio:
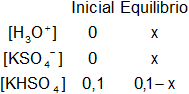
Aplicamos la constante de equilibrio para un ácido (kₐ):
![]()
Reemplazamos por los datos:
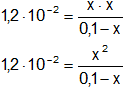
1,20·10⁻²·(0,1 - x) = x²
Igualamos a cero:
x² - 1,20·10⁻²·(0,1 - x) = 0
Aplicamos distributiva del producto con respecto a la resta:
x² + 1,20·10⁻²·x - 1,20·10⁻³ = 0
x² + 0,012·x - 0,0012 = 0
Aplicamos la ecuación de Báscara o Bhaskara:
![]()
Siendo:
a = 1
b = 0,012
c = -0,0012
Reemplazamos y resolvemos, obtendremos dos valores:

Calculamos los valores de x1,2 por separado según el signo del resultado de la raíz:
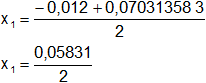
x₁ = 2,92·10⁻² mol/l
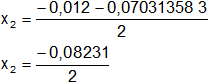
x₂ = -4,12·10⁻² mol/l (se descarta por < 0)
Respuesta: la concentración del ion hidronio de una solución de KHSO₄ 0,1 M es 2,9·10⁻² mol/l.
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP05
- | Siguiente ›
Ejemplo, cómo calcular la concentración dada la constante de ionización