Problema nº 3 de gases ideales, presión final de un gas - TP03
Enunciado del ejercicio nº 3
200 cm³ de un gas están sometidos a una presión de 2 atmósferas y a una temperatura de 40 °C, ¿qué presión ejerce si se lo calienta a 100 °C y se mantiene constante el volumen?
Desarrollo
Datos:
V₁ = 200 cm³ = 0,2 dm³
T₁ = 40 °C = 313 K
T₂ = 100 °C = 373 K
p₁ = 2 atm
Fórmulas:
![]()
Solución
El volumen permanece constante, por lo tanto, la ecuación general de los gases ideales queda:
![]()
Despejamos p₂ de la ecuación:
![]()
Reemplazamos por los datos y calculamos:
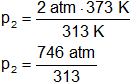
p₂ = 2,383386581 atm
Resultado, la presión que ejerce el gas es:
p₂ = 2,38 atm
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP03
- | Siguiente ›
Ejemplo, cómo determinar la presión final de un gas