Problema nº 9 de ecuación general de los gases ideales, presiones parciales de una mezcla de gases - TP16
Enunciado del ejercicio nº 9
Una mezcla de gas a 760 mm Hg de presión contiene 65 % de nitrógeno, el 15 % de oxígeno y 20 % de dióxido de carbono en volumen. ¿Cuál es la presión parcial de cada gas?
Desarrollo
Datos:
p = 760 mm Hg
N₂ = 65 %
O₂ = 15 %
CO₂ = 20 %
Fórmulas:
pT = ∑pg
Solución
Armamos la tabla de contingencia:
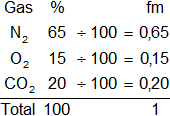
Aplicamos la ecuación de de las presiones parciales de los gases:
pT = ∑pg
Armamos la tabla de contingencia:
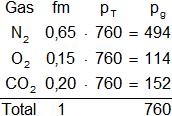
Resultado, la presión parcial de cada gas es:
pN₂ = 494 mm Hg
pO₂ = 114 mm Hg
pCO₂ = 152 mm Hg
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP16
- | Siguiente ›
Ejemplo de cómo calcular las presiones parciales de una mezcla de gases