Problema nº 3 cálculo de composición centesimal de una sustancia - TP07
Enunciado del ejercicio nº 3
Sabiendo que 5 g de agua están formados por 4,44 g de O y 0,56 g de H, hallar su composición centesimal.
Desarrollo
Datos:
magua = 5 g
mO = 4,44 g
mH = 0,56 g
Solución
La masa de la sustancia equivale al 100 %.
Aplicamos regla de tres simple y calculamos el porcentaje de cada componente.
Para el oxígeno:

Resultado, el porcentaje de oxígeno es:
xO = 88,8 %
Para el hidrógeno:
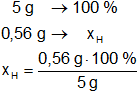
Resultado, el porcentaje de hidrógeno es:
xH = 11,2 %
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP07
- | Siguiente ›
Ejemplo, cómo calcular la composición centesimal de una sustancia