Problema nº 4 cálculo de composición centesimal de una sustancia - TP07
Enunciado del ejercicio nº 4
Al descomponer 216,6 g de óxido mercurioso (HgO), se forman 200,6 g de Hg y 16,0 g de O, hallar su composición centesimal.
Desarrollo
Datos:
msustancia = 216,6 g
mHg = 200,6 g
mO = 16 g
Solución
La masa de la sustancia equivale al 100 %.
Aplicamos regla de tres simple y calculamos el porcentaje de cada componente.
Para el mercurio:
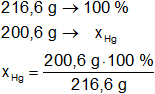
Resultado, el porcentaje de mercurio es:
xHg = 92,61 %
Para el oxígeno:
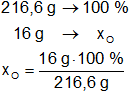
Resultado, el porcentaje de oxígeno es:
xO = 7,39 %
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP07
- | Siguiente ›
Ejemplo, cómo calcular la composición centesimal de una sustancia