Problema nº 4 de estequiometría de las disoluciones, soluto y solvente - TP02
Enunciado del ejercicio nº 4
Se quiere preparar una solución de sal en agua de forma que la concentración sea de 15 g de sal en 100 g de agua, se dispone de 50 g de sal, calcular:
a) ¿Qué cantidad de solución se puede preparar?
b) ¿Cuánta agua se precisa?
Desarrollo
Datos:
C = 15 g de sal en 100 g de agua
Sal = 50 g (soluto)
Solución
a)
La concentración requerida de la solución es de 15 g de sal en 100 g de agua, por lo tanto, la masa será de 115 g.
Aplicamos regla de tres simple:
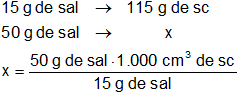
Resultado, la cantidad de solución que se puede preparar es:
x = 383,33 g
b)
En éste caso, la concentración requerida de la solución es de 15 g de sal en 100 g de agua, para 50 g de sal será:
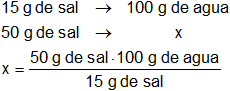
Resultado:
x = 333,33 g de agua
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP02
- | Siguiente ›
Ejemplo, cómo calcular el soluto y el solvente en una disolución