Problema nº 1 de fórmula mínima y molecular - TP07
Enunciado del ejercicio nº 1
Sabiendo que la composición centesimal de una sustancia es: C = 27,2727 %; O = 72,7272 % y los pesos atómicos son C = 12 y O = 16, calcular la fórmula mínima y la fórmula molecular si el peso molecular de la sustancia es 44 g.
Desarrollo
Datos:
msustancia = 100 g
C = 27,2727 %
O = 72,7272 %
Masa atómica C = 12
Masa atómica O = 16
Mol = 44
Solución
La masa de la sustancia equivale al 100 % por tanto:
C = 27,2727 % ≡ 27,2727 g
O = 72,7272 % ≡ 72,7272 g
Calculamos el número de átomos gramos de cada componente que hay en los 100 g de sustancia:
![]()
![]()
![]()
![]()
El número de átomos gramos de cada elemento debe ser entero, dividimos por el menor valor:
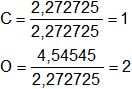
Respuesta, la fórmula mínima es: C₁O₂
Para calcular la fórmula molecular empleamos el peso molecular de la sustancia con la la fórmula mínima:
Peso molecular = 12·1 + 16·2
Peso molecular = 12 + 32
Peso molecular = 44
Respuesta, la fórmula molecular es: CO₂
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP07
- | Siguiente ›
Ejemplos de cómo calcular la fórmula mínima y la fórmula molecular