Otras rutas de utilización de la glucosa
Ciclo del glioxilato
Es la única manera de obtener glucosa a partir de C₂, normalmente el acetil-CoA. En células animales el paso de C₃ a C₂ está muy restringido. En el ciclo del glioxilato a partir de dos moléculas C₂ se obtiene un C₄ que se descarboxila y se obtiene un C₃. Este ciclo es muy importante en semillas para almacenar más cantidad de energía en menos espacio, en forma de grasas en lugar de ser hidratos de carbono. Las grasas al degradarse lo hacen en forma de C₂, por lo que tienen que ser capaces de utilizarlos para obtener todos los hidratos de carbono que necesiten. Este ciclo se realiza en el glioxisoma y es una variación del ciclo de Krebs.
Balance neto: 2 acetil-CoA ⟶ 1 succinato.
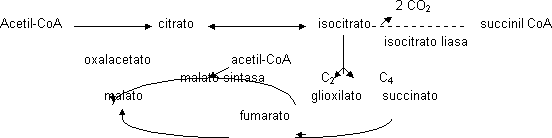
En este ciclo a partir del isocitrato actúa un enzima distinto, ya que debe romperse, la isocitrato liasa. Da lugar a 1 C₄ (succinato)+ 1 C₂ (glioxilato). El glioxilato puede aceptar otra molécula de acetil-CoA formando malato gracias a la malato sintasa. Tanto el isocitrato liasa como el malato sintasa se sintetizan cuando se necesitan.
Ruta de los fosfatos de pentosa
Es una ruta secundaria pero muy importante que existe en todas las células, Tiene lugar en el citosol. Permite obtener pentosas fosforiladas que se usan para sintetizar nucleótidos ya que es la fuente de ribosa necesaria. También se forma NADPH que es el poder reductor. La glucosa al entrar en la célula es G6P y por medio de la G6Pasa se convierte en fosfoglucono lactona con reducción de NAD⁺

La fosfoglucono lactona se hidroliza con la lactonasa, obteniendo fosfogluconato que se descarboxila oxidativamente. Actúa una deshidrogenasa dependiente del NADP⁺. Al descarboxilarse se obtiene un C₅, la ribulosa 5P que es fuente de energía de la ribosa 5P. La célula necesita más poder reductor que 5 C, como le sobran azúcares de 5 C los utiliza para regenerar los productos de 6 C. Por esto tendrá que ocurrir 6 veces el ciclo para la degradación total de una molécula de glucosa. Si la reacción ocurre 6 veces:
| 6·G6P ⟶ 6·C₅ ⟶ | 12·NADPH + 6·CO₂ + 6·Ru5P 5·C₆P |
| 6·G6P + 6·C₅P ⟶ En total: 1 G6P ⟶ | 12·NADPH + 6·CO₂ + 6·C₅P + 5·C₆P 12·NADPH + 6·CO₂ |
Intervienen varios tipos de enzimas:
- Isomerasas
- Epimerasas: transforman un epímero en otro
- Transacetolasas (TC): catalizan transferencias de C₂
- Transaldolasas (TA): catalizan transferencias de C₃ siempre de cetosa a aldosa
Cuando el ciclo ha dado 6 vueltas tenemos 6Ru5P que se han de transformar en 5 de G6P.
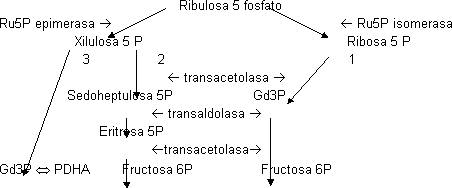
Esta ruta es esencial, se da en el citosol de todas las células
Fijación autotrófica del CO₂
El CO₂ es la forma más oxidada del C. Los organismos fotosintéticos son los únicos capaces de sintetizar una molécula reducida a partir de una oxidada (el CO₂ atmosférico). Para la síntesis requiere ATP y poder reductor (lo que hemos formado anteriormente). En eucariotas esto se produce en el estroma del cloroplasto (porción soluble). El proceso acaba al sintetizar una triosa fosfato que tras salir al citosol se convierte en glucosa como antes. La forma de transportar la glucosa por la planta es en forma de sacarosa, que se forma en el citosol.
Normalmente el proceso es igual para todas las células, el ciclo de Calvin. Se usó CO₂ marcado radioactivamente y se comprobó que la primera molécula marcada era una molécula de 3 carbonos por lo que se las llamó plantas C₃. Este resto se identificó como 3-fosfoglicerato. El CO₂ no es aceptado por un C₂ sino que se une a un C₅ y luego se rompe en dos C₃. El C₆ no se separa nunca de la enzima.
Ciclo de Calvin
Primera etapa: carboxilación
| (CH₂OP)—(CO)—(HCOH)₂—(CH₂OP) Ribulosa 1,5 bifosfato | + CO₂ ⟶ RUBISCO | 2X {(COO⁻)—(CHOH)—(CH₂OP) 3-fosfoglicerato |
La RUBISCO es el único enzima de este ciclo no presente en animales. Es una proteína muy importante en células vegetales y está sometido a regulación. Tiene subunidades catalíticas (L) y reguladoras (S) más pequeñas. Muy abundante en cloroplastos, hasta el 50 % del peso de hoja fresca (más abundante en el mundo). Tal cantidad hace pensar que se use de reserva, por ejemplo de N dada la gran cantidad de aminoácidos.
Las reacciones son termodinámicamente favorables, aunque la enzima presenta un problema, que puede usar O₂ también de sustrato. El CO₂ y el O₂ compiten por el sitio activo, la enzima tendrá actividad carboxilasa y oxigenasa. Si oxigena rompe en 2 la molécula:
| (CH₂OP)—(CO)—(HCOH)₂—(CH₂OP) Ribulosa,5 bifosfato | +O₂ ⟶ RUBISCO | (CH₂OP)—(COO⁻) + Fosfoglicolato | (CH₂OH)—(HCOH)—(CH₂OP) Fosfoglicerato |
Segunda etapa: fase reductiva
Transformar 3PG en Gd3P. Misma reacción que en la gluconeogénesis.
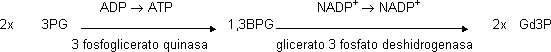
ATP y NADP⁺ producido acoplados a la cadena de transporte fotoelectrónico. Hasta ahora sólo 1 carbono procede del CO₂, por lo que ha de dar 3 vueltas para que todos sean del CO₂
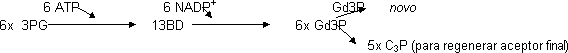
| 3x Ru1,5BP + 3·CO₂ ⟶ | 6x 3PG RUBISCO |
Segunda etapa: regeneración del aceptor final
5·C₃P ⟶ 3·C₅P. Cada C₅P se ha de fosforilar para que sean bifosfato por medio de una quinasa.
Los enzimas que son distintos son: fosforibulosa quinasa, RUBISCO y sedorribulosa-1,7-bifosfatasa.
Balance neto: 3·CO₂ ⟶ 6 ATP (de fosforilar 3PG) + 3 ATP (de fosforilar Ru5P)
3·CO₂ + 9 ATP + 6 NADPH ⟶ triosa fosfato + 6 NADP⁺ + 9 ADP
Regulación del ciclo de Calvin
Sólo ocurre cuando hay luz porque hace falta NADPH y ATP. La regulación asegura la fijación de CO₂ cuando hay luz y funciona la cadena de transporte fotoelectrónico. Regulación a nivel de RUBISCO a varios niveles relacionados con el período luminoso.
La actividad de RUBISCO depende de:
- Si el pH sube se activa. Si la cadena de transporte fotoelectrónico funciona se bombean H⁺ dentro del tilacoide y el pH sube en el estroma donde RUBISCO es activa. ΔμH = ΔΨ (potencial de membrana) + ΔpH (gradiente de concentración). En el cloroplasto ΔΨ es poco importante porque se transportan H⁺ pero se sacan Mg²⁺ y no se crea potencial. Al aumentar la concentración de Mg²⁺ aumenta la actividad
- Si sube la concentración de Mg²⁺ se activa
- Si sube la concentración de NADPH se activa. La cadena de transporte fotoelectrónico produce NADPH
Relacionados con la fase luminosa mediante la cadena de transporte fotoelectrónico de la membrana tilacoidal.
Otra regulación más general (de todos los procesos del cloroplasto) activado por F6P e inhibido por F1,6BP. Se pueden interconvertir por medio de la F1,6Bifosfatasa, enzima de la gluconeogénesis. Está reglado por la luz mediante el poder reductor. Al funcionar la cadena de transporte fotoelectrónico aumenta el poder reductor en el cloroplasto. En muchos procesos la estabilidad del mensajeros es el regulador y depende del estado redox. Tienen todas las cisteínas de dos maneras, formando puentes disulfuro o no. La forma SH es la reducida, muchas proteínas deben estar reducidas para funcionar. Para pasar de oxidada a reducida necesitaremos e⁻ de la cadena de transporte fotoelectrónico vía ferredoxina. La quinasa del final está igual regulada.
Fotorrespiración
Es el consumo de O₂ en presencia de luz. Este problema es resultado de la actividad oxigenasa de la RUBISCO. Si no hay luz RUBISCO está inactiva.
Balance neto: el O₂ se consume y se desprende CO₂, lo opuesto a lo deseado en la fotosíntesis. No se produce energía, se reduce la eficiencia de la fotosíntesis. Problema para la agricultura porque aparece menos biomasa. RUBISCO 2 actividades y una molesta porque la conformación de la enzima hace que pueda aceptar O₂, aunque es más afín por el CO₂. Si la fotosíntesis es contínua aumenta mucho la concentración de O₂ y disminuye la concentración de CO₂ por lo que se convierte en un competidor peligroso.
Defensa: km < CO₂, la km es alta para CO₂. Nadie sabe la utilidad de la función oxigenasa. Al principio no había O₂ en la atmósfera con lo que no era un problema.
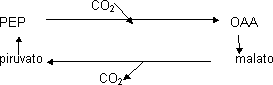
Algunas plantas disminuyen la actividad oxigenasa porque separan espacialmente las 2 fases de la fotosíntesis. En la zona donde se transportan e⁻ se produce O₂ y en la zona de actividad de RUBISCO se consume. Las hojas tienen una anatomía especial, tienen células donde se transportan e⁻ y otras con actividad de RUBISCO. Las células del mesófilo de la hoja fijan CO₂ temporalmente, pero no por RUBISCO. PEP recoge el CO₂ (PEP carboxilasa). Al fijar CO₂ se forma OAA que se transforma en malato que viaja a las células donde está RUBISCO. El malato ahora se descarboxila, produce C₃ (piruvato) y resulta CO₂. Donde es activa la RUBISCO la concentración de CO₂ aumenta y la concentración de O₂ disminuye. La fijación es favorecida. El piruvato vuelve a la otra célula y se transforma en PEP. Al marcar radioactivamente aparece primero OAA, por lo que se llaman plantas C₄ (CO₂ fijado en un C₄). La molécula de 4 carbonos sólo transporta el CO₂ hasta RUBISCO. De este tipo son muchas plantas tropicales.
En otras plantas la separación es temporal, aunque son C₄ igualmente. Por la noche se abren los estomas que fijan el CO₂ igual que en el caso anterior (la luz no es necesaria). Por el día cierra los estomas liberando el CO₂. Son plantas tropicales.
Metabolismo de polisacáridos
En las células animales la glucosa se almacena en forma de glucógeno y en las vegetales en forma de almidón. El glucógeno es un polisacárido formado por glucosas unidas por medio de enlaces glicosídicos α1 ⟶4. Las ramificaciones están unidas por enlaces α1 ⟶6. Tiene un extremo reductor y otro no reductor. El no reductor es en la cadena α1 ⟶4 el que no ofrece el C₁
Que la molécula está ramificada es una ventaja porque así tiene muchos extremos no reductores a la vista. También es más soluble. Forma gránulos en el citosol en los que normalmente están añadidos los enzimas que lo metabolizan dos tipos de células almacenan glucógeno, las musculares y las hepáticas, aunque para funciones distintas.
Glucogenolisis
Estudiada por Carl Ferdinand Cori y Gerty Theresa Radnitz. Se puede hidrolizar el enlace, pero en la célula se hace por medio de un fosfato (fosforolisis). La ventaja es que se obtiene glucosa ya fosforilada por lo que no tiene que actuar la hexoquinasa:
| (Glu)ₙ + Pi ⟶ | G1P + (Glu)₍ₙ ₋ ₁₎ Glucógenofosforilasa |
Se degrada siempre empezando por el extremo o reductor rompiendo los enlaces glicosídicos α1 ⟶4. El enzima no puede degradar completamente el glucógeno, al llegar al extremo hay repulsiones estéricas. Se para a 4 residuos de la ramificación. Necesita otro enzima con 2 actividades enzimáticas:
- Transferasa α1 ⟶4: coge los 2 primeros y los transfiere a un extremo no reductor
- Glicosidasa: coge el residuo del punto de ramificación con enlace α1 ⟶6 y lo hidroliza quedando una glucosa sin fosforilar. Las glucosas almacenadas aparecen todas fosforiladas menos las de las ramificaciones
Para degradar las glucosas han de aparecer intermediarios de la glicolisis, la mayor parte G1P:
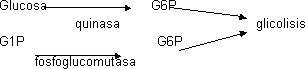
Al movilizar el hígado el glucógeno libera glucosa y G1P que para salir de la célula ha de perder el fosfato, se transforma primero en G6P y con enzima G6fosfatasa (de la gluconeogénesis) elimina el P. La G6Pasa salva el paso de la fosfoquinasa.
Glucogenogénesis
Requiere extremo no reductor para incorporar las glucosas por ese lado. El enzima es la glucogenosintasa. Estudiado por el bioquímico argentino Luis Federico Leloir. La glucosa debe estar activada combinándola con nucleótidos (derivado de la uridina, UTP). Activación:
| Glucosa ⟶ | G6P ⇔ | G1P + UTP Hexoquinasa | |
| G1P + P-P-P-uridina | ⟶ | UDP-glucosa. UDP glucosapirofosforilasa | + PPi |
Siempre que el pirofosfato sea un producto la reacción va hacia la derecha. El enzima glucogenosintasa añade resto de glucosa formando α1 ⟶4 y libera UDP. Punto de control más importante. El UDP se necesita como UTP por lo que para recuperarlo se necesita ATP por medio de una nucleósido difosfoquinasa.
Para las ramificaciones coge un trozo ya sintetizado de unos 7 monómeros y lo mueve hacia dentro de la cadena (unas 11 glucosas). Se transfiere entero en posición 6 a una glucosa ya unida. De esto se ocupa una transferasa. Ahora una sintasa une por los 2 sitios. La separación entre ramas es de por lo menos 4 glucosas para poder degradarlo luego.
| (Glu)ₙ + UDP-Glu ⟶ | (Glu)₍ₙ ₊ ₁₎ Glucógeno sintasa |
La glucógeno sintasa siempre necesita cebador (extremo no reductor). Casi siempre el cebador es el glucógeno que no se degrada del todo nunca. Para sintetizar desde cero el cebador es una proteína que se puede glicosidar (añadir azúcar). El azúcar se une a los OH de Ser y Thr formando un enlace glicosídico.
Regulación
El glucógeno está almacenado en el citosol donde se hallan los enzimas encargados de degradarlo y sintetizarlo. Las 2 rutas no pueden funcionar al revés.
La síntesis implica activar glucogenosintasa cuando haya mucha glucosa. Si la concentración de glucosa es alta no es necesario movilizar las reservas. La degradación ocurre al bajar el nivel de glucosa (es el modulador). Estos dos procesos nunca son activos a la vez.
Células hepáticas
La glucogenofosforilasa está regulada por:
Modificación covalente, por lo que puede existir en dos formas, la no fosforilada es inactiva.
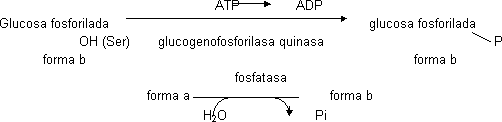
La forma b está regulada alostéricamente. Modulador positivo concentración de AMP alta (falta ATP). Si la concentración de AMP es alta pasa a la forma a.
Si la concentración de glucosa baja el glucógeno se degrada y la glucosa pasa a la sangre. Modulación regulada por hormonas, que son moléculas señalizadores de organismos pluricelulares, producidas en algunos sitios para advertir de determinadas cosas. La concentración de glucosa e sangre dispara la producción de algunas hormonas que actúan sólo sobre células que tengan el receptor específico. Al llegar la hormona la célula desencadena una respuesta.
- Tras comer aumenta la concentración de glucosa en la sangre y se produce insulina por el páncreas. La insulina potencia la síntesis de glucógeno. Si hay insulina la glucógeno sintasa está activa y la fosforilasa no
- Entre comidas se produce glucagón que favorece la degradación activando la fosforilasa
Para coordinar ambos procesos la señal ha de ser la misma.
Al producirse glucagón algunas células con receptores, entre ellas las hepáticas, lo recogen. Al unirse al receptor cambia el metabolismo celular y desencadena el aumento de otro mensajero, el cAMP (3' y 5' unidos). Esto es porque la hormona no puede entrar dentro de la célula. Se favorece la síntesis de cAMP por la adenilato ciclasa que a partir de ATP sintetiza cAMP. Activación mediada por proteínas muy importantes llamadas proteínas G, que pueden unir GTP. Transmiten señales dentro de la célula y tienen 3 tipos de cadenas: α, β y γ.
α: une GDP ó GTP. Es activa cuando une GTP. La proteína G se autorregula porque hidroliza GTP (es GTPasa) en la cadena α. La proteína G media el efecto entre el receptor y la adenilato ciclasa. El receptor favorece el paso a forma activa. Al unirse la hormona y r receptor, la proteína G, que también está en la membrana, pasa a activa y pone en marcha a la adenilato ciclasa. La proteína G es activa hasta que se hidrolice el GTP. El cólera produce diarreas debido a una toxina que bloquea la actividad GTPasa de la proteína G, que ya no puede desconectarse, y no para de transportar iones y H₂O hasta la deshidratación.
El cAMP actúa de modulador para la proteínquinasa. Está formada por 2 subunidades catalíticas y 2 reguladoras cuando está inactiva (L₂R₂). El cAMP se une a las R que se separan de las catalíticas y la molécula queda activada. La proteínquinasa puede modificar a la glucógeno fosforilasa quinasa, que puede estar fosforilada o no. A expensas del ATP modifica la enzima activándolo, lo que inicia la cascada enzimática disparada por una hormona activa cuando la concentración de glucosa es baja.
La PKA puede fosforilar la glucógenosintasa que pasa a inactiva. Al activar PKA se pone en marcha una y para la otra.
Para invertir el efecto de una quinasa actúa una fosfatasa (que también está regulada). La fosfatasa es activa si la concentración de glucosa aumenta, desfosforila la enzima bloqueando un proceso timina empezando el otro.
cAMP puede romperse para que desaparezca la señal pasando a AMP y no activa la proteínquinasa. El enzima que lo rompe es la fosfodiesterasa.
Células musculares
El glucógeno se almacena para consuma propio de la célula. El glucagón no actúa sobre las células musculares. La cascada enzimática es la misma pero disparada por la adrenalina. El músculo necesita mucho ATP, requiere glucosa. Un esfuerzo continuado moviliza el glucógeno igual que antes. Las señales que determinan la contracción muscular son cambios en la concentración de iones. Al aumentar la concentración de Ca²⁺ dentro de la célula se activa la degradación de glucógeno (coordinando los dos procesos de lisis y síntesis). El Ca²⁺ activa la glucógeno fosforilasa quinasa uniéndose a la subunidad calmodulina. El efecto de la adrenalina es adelantarse a la situación teniendo ya preparada la glucosa antes de que la concentración de Ca²⁺ aumente.
Editor: Ricardo Santiago Netto (Administrador de Fisicanet).
Células hepáticas y musculares