Problema nº 5-e de ecuaciones de óxido reducción neta, igualación en forma iónica neta - TP04
Enunciado del ejercicio nº 5-e
Balancee la siguiente ecuación después de haberla expresado en forma iónica neta:
CO(g) + I₂O₅(g) ⟶ CO₂(g) + I₂(g)
Solución
Reacción de oxidación del monóxido de carbono por el óxido yódico con formación de dióxido de carbono y yodo libre.
CO(g) + I₂O₅(g) ⟶ CO₂(g) + I₂(g)
La siguiente reacción se realiza en estado gaseoso.
Los óxidos siempre se escriben en forma molecular.
CO + I₂O₅ ⟶ CO₂ + I₂°
El CO pasa a CO₂, el C se oxida, cede 2 electrones.
El I₂O₅ pasa a I₂°, el I se reduce, capta 5 electrones.
Presentamos en la ecuación solo los iones o moléculas que intervienen en la oxidación-reducción, es decir en forma iónica neta.
CO + I₂O₅ ⟶ CO₂ + I₂°
Resulta igual que la reacción inicial.
Resolvemos por el método del número de oxidación.
C²⁺ + O²⁻ + 2·I⁵⁺ + 6·O²⁻ ⟶ C⁴⁺ + 2·O²⁻ + I₂°
Semirreacción de reducción:
2·I⁵⁺ ⟶ I₂°
Equilibramos los electrones:
2·I⁵⁺ + 10·e ⟶ I₂° (1)
Semirreacción de oxidación:
C²⁺ ⟶ C⁴⁺
Equilibramos los electrones:
C²⁺ - 2·e ⟶ C⁴⁺ (2)
Se conserva la clase y la masa de los elementos (Ley de Lavoisier), sus cargas no cuentan.
El balance de la carga está equilibrado en cada semirreacción.
La ecuación completa es (1) y (2):
![]()
Multiplicamos apropiadamente las ecuaciones para poder simplificar los electrones:
![]()
Sumamos las ecuaciones miembro a miembro:
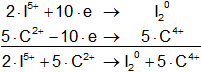
2·I⁵⁺ + 5·C²⁺ ⟶ I₂° + 5·C⁴⁺
La ecuación queda igualada.
Escribimos la reacción completa con los nuevos coeficientes:
5·CO + I₂O₅ ⟶ 5·CO₂ + I₂
Observar que los coeficientes hallados se colocaron sólo en los compuestos donde ocurrió oxidación y reducción.
La ecuación completa queda igualada.
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP04
- | Siguiente ›
Ejemplo, cómo igualar ecuaciones redox en forma iónica neta