Problema nº 9 de estequiometría de las disoluciones, neutralización de soluciones - TP02
Enunciado del ejercicio nº 9
¿Qué volumen de solución 0,1 N de KOH son necesarios para neutralizar totalmente a 25 cm³ de solución 0,5 N de H₂SO₄?
Solución
Método razonado
La ecuación estequiométrica balanceada es la siguiente:
2·KOH + H₂SO₄ ⟶ K₂SO₄ + 2·H₂O
Calculamos las masas de los moles que intervienen en la reacción en equilibrio:
2·KOH: 2·(39 g + 16 g + 1 g) = 112 g
H₂SO₄: 2·1 g + 32 g + 4·16 g = 98 g
K₂SO₄: 2·39 g + 32 g + 4·16 g = 174 g
2·H₂O: 2·(2·1 g + 16 g) = 36 g
![]()
Calculamos los equivalentes gramo.
El equivalente gramo del ácido sulfúrico es su mol dividido la cantidad de átomos de hidrógeno que posee en su mol.
![]()
Eg = 49 g (H₂SO₄)
El equivalente gramo del hidróxido de potasio es su mol dividido la cantidad de oxhidrilos que posee en su mol.
![]()
Eg = 56 g (KOH)
Calculamos la masa de ácido sulfúrico que hay en 25 cm³ de solución 0,5 N:
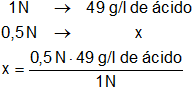
x = 24,5 g de ácido/l
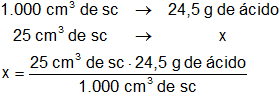
x = 0,6125 g de H₂SO₄ (puro)
Calculamos la masa de hidróxido de potasio necesaria para neutralizar 0,6125 g de ácido, de la ecuación estequiométrica tenemos:
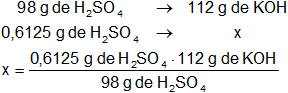
x = 0,7 g de KOH (puro)
Calculamos la masa de hidróxido de potasio que hay en una solución 0,1 N:
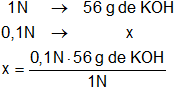
x = 5,6 g de KOH/l
Finalmente calculamos el volumen de solución que contiene 0,7 g de KOH:
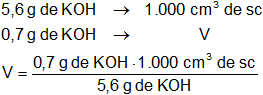
Resultado, el volumen de solución 0,1 N de KOH necesario para neutralizar 25 cm³ de solución 0,5 N de H₂SO₄ es:
x = 125 cm³
Método sencillo
De otro modo, mucho más sencillo, teniendo en cuenta que "se neutraliza equivalente gramo a equivalente gramo" y que:
V₁·N₁ = V₂·N₂
Despejamos V₁:
![]()
Reemplazamos por los datos y calculamos:
![]()
V₁ = 125 cm³
Mismo resultado.
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP02
- | Siguiente ›
Ejemplo, cómo calcular el volumen de neutralización en soluciones normales