Problema nº 6 de estequiometría de las disoluciones, equivalentes gramo - TP03
Enunciado del ejercicio nº 6
Calcular, sin emplear pesos atómicos, cuántos equivalentes gramo hay en:
a) 300 ml de solución 3 N de un ácido.
b) 3 dm³ de solución 0,3 N de un hidróxido.
c) 4 dm³ de solución 0,5 N de una sal.
Solución
a)
Por definición sabemos que:
![]()
Calculamos los equivalentes en 300 cm³:
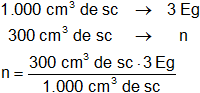
Resultado, los equivalentes gramo de ácido que hay en 300 cm³ de la solución 3 N es:
x = 0,9 Eg
b)
Por definición sabemos que:
![]()
Calculamos los equivalentes en 3.000 cm³:
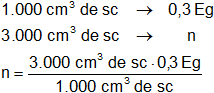
Resultado, los equivalentes gramo de hidróxido que hay en 3.000 cm³ de la solución 0,3 N es:
x = 0,9 Eg
c)
Por definición sabemos que:
![]()
Calculamos los equivalentes en 4.000 cm³:
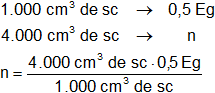
Resultado, los equivalentes gramo de sal que hay en 4.000 cm³ de la solución 0,5 N es:
x = 2 Eg
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP03
- | Siguiente ›
Ejemplo, cómo calcular los equivalentes gramo en una solución