Problema nº 5 de estequiometría de las disoluciones, volumen y peso específico - TP08
Enunciado del ejercicio nº 5
Calcular el volumen de ácido sulfúrico concentrado, de peso específico relativo 1,84 y contenido 98 % de H₂SO₄ en peso, que contendrá 40 g de H₂SO₄ puro.
Desarrollo
Datos:
mH₂SO₄ = 40 g
CSc = 98 %
ρᵣ = 1,84
Fórmulas:
![]()
Solución
Al tratarse de una disolución (sc) peso en peso, la masa de ácido sulfúrico es directamente 98 g por 100 g de disolución.
Calculamos la masa de disolución para 40 g de H₂SO₄ puro:
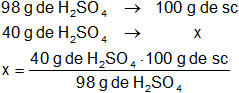
x = 40,81632653 g de Sc
Aplicamos la fórmula de peso específico relativo y la desarrollamos:
![]()
La densidad es:
![]()
Reemplazamos:
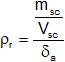
δₐ = 1 (agua)
La masa msc es constante, despejamos Vsc:
![]()
Reemplazamos por los valores y calculamos:
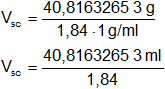
Vsc = 22,18278616 ml de Sc
Resultado, el volumen de ácido sulfúrico concentrado es:
Vsc = 22,2 ml de Sc
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP08
- | Siguiente ›
Ejemplo, cómo calcular el volumen de una disolución dado el peso específico