Problema nº 5, constante de equilibrio químico, moles - TP01
Enunciado del ejercicio nº 5
La constante de equilibrio para la siguiente reacción es 0,0045:
N₂ + O₂ ⇌ 2·NO
¿Cuántos moles de NO existirán en el equilibrio, si se combinan 3 moles de oxígeno y 3 moles de nitrógeno en un total de 20 litros?
Desarrollo
Datos:
K = 0,0045
Moles O = 3
Moles N = 3
V = 20 l
Solución
La ecuación equilibrada dada:
N₂ + O₂ ⇌ 2·NO
Calculamos la concentración de cada compuesto en 20 l. Para el oxígeno:
![]()
Para el nitrógeno:
![]()
Para el monóxido de nitrógeno (óxido de nitrógeno II):
![]()
En el equilibrio:
![]()
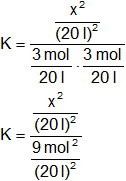
Simplificamos los denominadores:
![]()
Despejamos la concentración del hidrógeno x:
x² = K·9 moles²
Reemplazamos por los datos y calculamos:
x² = 0,0045·9 moles²
x² = 0,0405 moles²
![]()
x = 0,201246118 moles
Respuesta: la cantidad de moles de monóxido de nitrógeno que hay en el sistema es 0,201
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP01
- | Siguiente ›
Ejemplo, cómo calcular los moles dada la constante de equilibrio