Problema nº 5 de equilibrio químico, moles - TP02
Enunciado del ejercicio nº 5
A cierta temperatura la constante de equilibrio para la reacción:
H₂ + Br₂ ⇌ 2·HBr
Es K = 60,5.
Los 3 componentes gaseosos de la mezcla en equilibrio están contenidos en un recipiente de 12 litros. Se encuentra que el recipiente contiene 10⁻⁴ moles de hidrógeno y 2·10⁻⁴ moles de bromo. Calcular el número de moles de bromuro de hidrógeno que hay en el recipiente.
Desarrollo
Datos:
K = 60,5
Moles H = 10⁻⁴
Moles Br = 2·10⁻⁴
V = 12 l
Solución
La ecuación equilibrada dada:
H₂ + Br₂ ⇌ 2·HBr
Calculamos la concentración de cada compuesto en 12 l. Para el hidrógeno:
![]()
Para el bromo:
![]()
Para el bromuro de hidrógeno:
![]()
En el equilibrio:
![]()
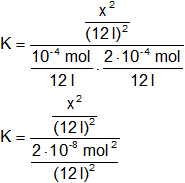
Simplificamos los denominadores:
![]()
Despejamos la concentración del bromuro de hidrógeno x:
x² = K·2·10⁻⁸ moles²
Reemplazamos por los datos y calculamos:
x² = 60,5·2·10⁻⁴ moles²
x² = 1,21·10⁻⁶ moles²
![]()
x = 0,0011 moles
Respuesta: la cantidad de moles de bromuro de hidrógeno que hay en el sistema es 1,1·10⁻³.
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP02
- | Siguiente ›
Ejemplo, cómo calcular los moles dada la constante de equilibrio