Problema nº 4 de estequiometria de las reacciones químicas, reactivos y productos - TP01
Enunciado del ejercicio nº 4
Se quieren preparar 3.000 kg de amoníaco a partir de la reacción:
N₂ + 3·H₂ ⟶ 2·NH₃
Calcular:
a) Volumen de nitrógeno medido en CNPT necesarios.
b) Masa de hidrógeno necesaria.
Desarrollo
Datos:
mamoníaco = 3.000 kg
CNPT
Solución
La ecuación de formación del anhídrido nítrico es la siguiente:
N₂ + 3·H₂ ⟶ 2·NH₃
Calculamos el mol de cada compuesto que interviene en la reacción:
N₂: 2·14,0067 g = 28,0134 g
3·H₂: 3·2·1,00797 g = 6,04782 g
2·NH₃: 2·(14,0067 g + 3·1,00797 g) = 34,06122 g
![]()
Recordemos que en CNPT el volumen que ocupa un mol de gas es 22,4 litros, por lo tanto:
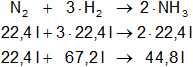
a)
Si 3.000 kg de amoníaco = 3.000.000 g, para calcular el volumen nitrógeno medido en CNPT:
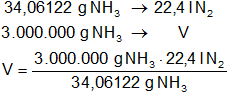
Resultado (a):
Vnitrógeno = 1.972.918,17 l de N₂
b)
Para calcular la masa hidrógeno:
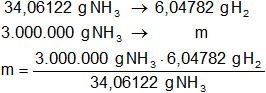
mhidrógeno = 532.672,053 g de H₂
Resultado (b):
mhidrógeno = 532,67 kg de H₂
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP01
- | Siguiente ›
Ejemplo de cómo determinar las cantidades de las sustancias reaccionantes y de los productos de reacción