Problema nº 11 de estequiometria de las reacciones químicas, reactivos y productos - TP02
Enunciado del ejercicio nº 11
Reaccionan 10 g de aluminio con 10 g de oxígeno, ¿cuál de los reactivos está en exceso? ¿cuántos gramos de óxido de aluminio se forman?
Desarrollo
Datos:
maluminio = 10 g
moxígeno = 10 g
Solución
La ecuación estequiométrica balanceada es la siguiente:
4·Al + 3·O₂ ⟶ 2·Al₂O₃
Calculamos el mol de cada compuesto que interviene en la reacción:
4·Al: 4·26,98 g = 107,92 g
3·O₂: 3·2·16 g = 96 g
2·Al₂O₃: 2·(2·26,98 g + 3·16 g) = 203,92 g
![]()
A simple viste se observa que el oxígeno está en exceso, verificamos.
Mediante regla de tres simple calculamos que masa de oxígeno necesaria para reccionar con 10 g de aluminio:
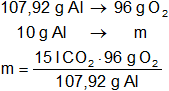
moxígeno = 8,9 g de O₂
Con el mismo método calculamos la masa de óxido de aluminio formado:
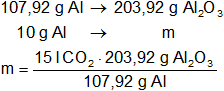
móxido de aluminio = 18,9 g de Al₂O₃
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP02
- | Siguiente ›
Ejemplo de cómo determinar las cantidades de las sustancias reaccionantes y de los productos de reacción