Problema nº 3 de estequiometria de las reacciones químicas, reactivos y productos - TP05
Enunciado del ejercicio nº 3
Se hace reaccionar 9,2 g de sodio metálico con cantidad suficiente de agua, calcular:
- El volumen de hidrógeno gaseoso producido en CNPT.
- Los gramos de agua que reaccionan.
Desarrollo
Datos:
mNa = 9,2 g
Solución
La ecuación estequiométrica balanceada es la siguiente:
2·Na + 2·H₂O ⟶ 2·NaOH + H₂
Calculamos el mol de cada compuesto que interviene en la reacción:
2·Na: 2·23 g = 46 g
2·H₂O: 2·(2·1 g + 16 g) = 36 g
2·NaOH: 2·(23 g + 16 g + 1 g) = 80 g
H₂: 2·1 g = 2 g
![]()
Calculamos el volumen de hidrógeno gaseoso producido:
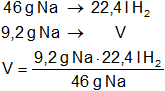
Resultado, el volumen de hidrógeno producido en CNPT es:
VH₂ = 4,48 l de H₂
Calculamos los gramos de agua que reaccionan:
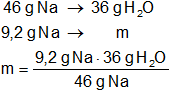
Resultado, los moles de agua requeridos son:
xH₂O = 7,2 g de H₂O
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP05
- | Siguiente ›
Ejemplo, cómo determinar las cantidades de las sustancias reaccionantes y de los productos de reacción