Problema nº 6 de estequiometria de las reacciones químicas, cantidades de las sustancias reaccionantes - TP05
Enunciado del ejercicio nº 6
Se desea preparar 210 g de ácido hipocloroso a partir de la reacción de su óxido y agua. ¿Cuántos gramos de óxido se necesitan?
Desarrollo
Datos:
mHClO = 210 g
Solución
La ecuación estequiométrica balanceada es la siguiente:
Cl₂O + H₂O ⟶ 2·HClO
Calculamos el mol de cada compuesto que interviene en la reacción:
Cl₂O: 2·35,5 g + 16 g = 87 g
H₂O: 2·1 g + 16 g = 18 g
2·HClO: 2·(35,5 g + 16 g + 1 g) = 105 g
![]()
Calculamos la masa de óxido hipocloroso necesaria:
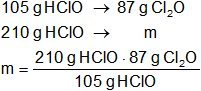
Resultado, la masa de óxido hipocloroso necesaria es:
mCl2O = 174 g de Cl₂O
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP05
- | Siguiente ›
Ejemplo, cómo determinar las cantidades de las sustancias reaccionantes