Problema nº 5 de gases ideales, cantidad de moléculas en un gas - TP01
Enunciado del ejercicio nº 5
¿Cuántos moles de CO₂ hay en 2,709·10²⁴ moléculas, indicar la masa, el volumen y la atomicidad de un mol.
Desarrollo
Datos:
MCO₂ = 2,709·10²⁴ moléculas
Vmol = 22,4 dm³ CNPT
Solución
Sabemos que en mol de cualquier gas en CNPT hay 6,02·10²³ moléculas.
a)
Calculamos la masa de un mol de CO₂:
PM de CO₂: 12,01115 g + 2·15,9994 g = 44,00995 g
Mediante regla de tres simple calculamos la cantidad de moles:
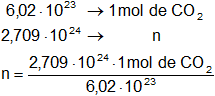
Resultado, los moles de CO₂ es:
n = 4,5 moles de CO₂
b)
Calculamos la masa de CO₂:
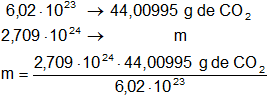
Resultado, la masa de CO₂ es:
m = 198,045 g de CO₂
c)
Calculamos el volumen de CO₂:
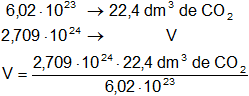
Resultado, el volumen de CO₂ es:
V = 198,045 dm³ de CO₂
d)
Resultado, la atomicidad de un mol de CO₂ es 3 heteroatómica
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP01
- | Siguiente ›
Ejemplo de cómo determinar la cantidad de moléculas en un gas