Problema nº 4 de ley de las proporciones múltiples - TP02
Enunciado del ejercicio nº 4
Al analizar los óxidos del cloro se obtiene:
Óxido I: Cl 81,59 %; O 18,41 %
Óxido II: Cl 59,63 %; O 40,37 %
Óxido III: Cl 46,98 %; O 53,02 %
Óxido IV: Cl 38,76 %; O 61,24 %
Demostrar que se cumple la ley de Dalton.
Solución
Realizamos las relaciones correspondientes entre las masas de cloro y las de oxígeno:
![]()
![]()
R₁ = 4,43
![]()
![]()
R₂ = 1,48
![]()
![]()
R₃ = 0,89
![]()
![]()
R₄ = 0,63
Verificamos la ley de las proporciones múltiples haciendo el cociente entre relaciones "R" halladas.
![]()
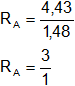
![]()
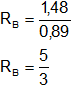
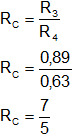
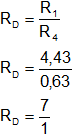
Se cumple la ley de las proporciones múltiples o ley de Dalton.
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP02
- | Siguiente ›
Ejemplo, cómo verificar la ley de las proporciones múltiples