Problema nº 5-c de ecuaciones de óxido reducción, equilibrar por el método del ion electrón - TP01
Enunciado del ejercicio nº 5-c
Igualar la siguiente ecuación por el método del ion electrón:
FeCl₃ + H₂S ⟶ FeCl₂ + S + HCl
Reacción de oxidación del ácido sulfhídrico por el cloruro férrico con formación de cloruro ferroso y azufre libre.
Solución
Primero disociamos los compuestos detallando el número de oxidación:
FeCl₃ + H₂S ⟶ FeCl₂ + S + HCl
Fe³⁺ + 3·Cl⁻ + 2·H⁺ + S²⁻ ⟶ Fe²⁺ + 2·Cl⁻ + S° + H⁺ + Cl⁻
Identificamos los elementos que se reducen y los que se oxidan. Recordar que si un elemento se reduce hay otro que se oxida.
El S²⁻ pasa a S°, se oxidó.
El Fe³⁺ pasa a Fe²⁺, se reduce.
Ahora armamos las hemireacciones:
![]()
Ahora equilibramos los electrones, si es necesario, sumando los signos +/- que hay de ambos lados del igual:
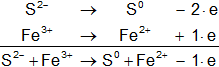
Hay que equilibrar los electrones, multiplicando cada hemireacción por el número opuesto de los electrones:
![]()
Calculamos:
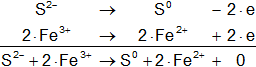
Volvemos a la primera ecuación y la armamos con los nuevos coeficientes:
2·FeCl₃ + H₂S ⟶ 2·FeCl₂ + S + HCl
Terminamos de equilibrar la ecuación:
2·FeCl₃ + H₂S ⟶ 2·FeCl₂ + S + 2·HCl
La ecuación queda igualada.
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP01
- | Siguiente ›
Ejemplo de equilibrar ecuaciones por el método del ion electrón