Problema nº 5-d de ecuaciones de óxido reducción, equilibrar por el método del ion electrón - TP01
Enunciado del ejercicio nº 5-d
Igualar la siguiente ecuación por el método del ion electrón:
K₂Cr₂O₇ + H₂SO₄ ⟶ K₂SO₄ + Cr₂(SO₄)₃ + H₂O + O₂
Reacción de reducción del dicromato de potasio por el ácido sulfúrico con formación de sulfato crómico y oxígeno libre.
Solución
Primero disociamos los compuestos detallando el número de oxidación:
K₂Cr₂O₇ + H₂SO₄ ⟶ K₂SO₄ + Cr₂(SO₄)₃ + H₂O + O₂
2·K⁺ + Cr₂O₇²⁻ + 2·H⁺ + SO₄²⁻ ⟶ 2·K⁺ + SO₄²⁻ + 2·Cr³⁺ + 3·SO₄²⁻ + H⁺ + OH⁻ + O₂°
Identificamos los elementos que se reducen y los que se oxidan. Recordar que si un elemento se reduce hay otro que se oxida.
El oxígeno del Cr₂O₇²⁻ pasa a O°, se oxidó.
El cromo del Cr₂O₇²⁻ pasa a Cr³⁺, se reduce.
Ahora armamos las hemireacciones:
![]()
Compensamos el hidrógeno y el agua:
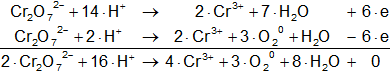
Volvemos a la primera ecuación y la armamos con los nuevos coeficientes:
2·K₂Cr₂O₇ + 8·H₂SO₄ ⟶ K₂SO₄ + 2·Cr₂(SO₄)₃ + 8·H₂O + 3·O₂
Terminamos de equilibrar la ecuación:
2·K₂Cr₂O₇ + 8·H₂SO₄ ⟶ 2·K₂SO₄ + 2·Cr₂(SO₄)₃ + 8·H₂O + 3·O₂
La ecuación queda igualada.
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP01
- | Siguiente ›
Ejemplo de equilibrar ecuaciones por el método del ion electrón