Problema nº 3-d de ecuaciones de óxido reducción, igualación dadas en forma iónica - TP04
Enunciado del ejercicio nº 3-d
Balancee la siguiente ecuación efectuada en medio acuoso:
H₃AsO₄ + H⁺ + Zn ⟶ AsH₃ + H₂O + Zn²⁺
Reacción de oxidación del cinc metálico por el ácido arsénico con formación de hidruro de arsénico.
Solución
La siguiente reacción se realiza en medio acuoso, hay compuestos que están representados en forma iónica e incompleta. Están presentes los elementos que se reducen y los que se oxidan. Nos enfocamos en ellos sin importar los iones o compuestos faltantes.
H₃AsO₄ + H⁺ + Zn ⟶ AsH₃ + H₂O + Zn²⁺
Identificamos los elementos e iones que se reducen y los que se oxidan.
El H₃AsO₄ pasa a AsH₃, se reduce, capta 8 electrones.
El Zn° pasa a Zn²⁺, se oxida, cede 2 electrones.
Armamos las semireacciones paso a paso.
Semirreacción de reducción:
H₃AsO₄ ⟶ AsH₃
Equilibramos los electrones:
H₃AsO₄ + 8·e ⟶ AsH₃
Agregamos el oxgíeno (presente en el agua) y lo equilibramos:
H₃AsO₄ + 8·e ⟶ AsH₃ + 4·H₂O
Luego, para compensar, agregamos el hidrógeno y lo equilibramos:
H₃AsO₄ + 8·e + 8·H⁺ ⟶ AsH₃ + 4·H₂O (1)
Semirreacción de oxidación:
Zn° ⟶ Zn²⁺
Equilibramos los electrones:
Zn° - 2·e ⟶ Zn²⁺ (2)
Se conserva la clase y la masa de los elementos (Ley de Lavoisier), sus cargas no cuentan.
El balance de la carga está equilibrado en cada semirreacción.
La ecuación completa es (1) y (2):
![]()
Multiplicamos apropiadamente las ecuaciones para poder simplificar los electrones:
![]()
Sumamos las ecuaciones miembro a miembro:
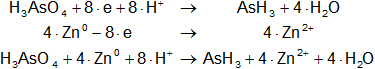
H₃AsO₄ + 4·Zn° + 8·H⁺ ⟶ AsH₃ + 4·Zn²⁺ + 4·H₂O
La ecuación queda igualada.
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP04
- | Siguiente ›
Ejemplo, cómo igualar ecuaciones redox dadas en forma iónica