Problema nº 5 de fórmula gramo - TP04
Enunciado del ejercicio nº 5
Se quieren tener 10 fórmulas gramo de Na₂HPO₄. ¿Qué masa debe tomarse?
Desarrollo
Datos:
mNa = 22,9898 g
mP = 30,9738 g
mH = 1,00797 g
mO = 15,9994 g
El mol es la suma de los pesos atómicos de todos los elementos que forman la molécula, en este caso una sal hidratada.
Solución
Calculamos el peso molecular del fosfato ácido de sodio, multiplicamos por la cantidad de átomos presentes en la sustancia y sumamos:
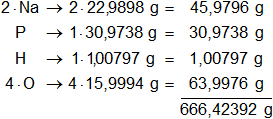
Una fórmula gramo o mol de Na₂HPO₄ pesa 141,95897 g, se necesitan 10 fórmulas gramo, entonces:
10 fórmulas gramo = 10·141,95897 g = 1419,5897 g
Respuesta: la masa necesaria de fosfato ácido de sodio es 1.419,59 g
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP04
- | Siguiente ›
Ejemplo, cómo calcular la fórmula gramo de un compuesto