Problema nº 6 de peso molecular y masa de una molécula - TP04
Enunciado del ejercicio nº 6
El S se combina con el H, dando un compuesto cuya fórmula es H₂S, calcular:
a) El peso molecular de dicho compuesto.
b) La masa de una molécula de dicho compuesto.
Desarrollo
Datos:
mH = 1,00797 g
mS = 32,064 g
1 mol ≡ 6,02·10²³ moléculas (número de Avogadro)
Para hallar el valor de una molécula gramo o mol de una sustancia debemos conocer el valor de los pesos atómicos relativos de los átomos que la forman.
El mol es la suma de los pesos atómicos de todos los elementos que forman la molécula.
Solución
a)
Calculamos el peso molecular del sulfuro de hidrógeno, multiplicamos por la cantidad de átomos presentes en la sustancia y sumamos:
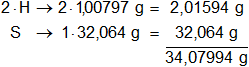
Respuesta a): el peso molecular del H₂S es 34,07994 g
b)
Calculamos masa de una molécula de sulfuro de hidrógeno:

x = 5,66·10⁻²³ g de H₂S
Respuesta b): la masa de una molécula de H₂S es 5,66·10⁻²³ g
Resolvió: Ricardo Santiago Netto. Argentina
- ‹ Anterior |
- Regresar a la guía TP04
- | Siguiente ›
Ejemplo, cómo calcular el peso molecular de una sustancia